Bevezetés
Az első őssejt-transzplantációt Donnel Thomas végezte az ötvenes években és Nobel-díjat kapott a beavatkozás kidolgozásáért. Akkor még a csontvelő (CSV) számított elsődleges őssejtforrásnak, és szinte kizárólag hematológiai kórképek gyógyítására használták. Alternatív őssejtforrásként merült fel később a köldökzsinórvér (KZSV), amivel az első transzplantációt 1988-ban végezték Párizsban, egy Fanconi-anaemiás gyermeknél, Prof. Gluckman és Dr. Broxmeyer vezetésével.
A mesenchymalis őssejteket (MSC) 1968-ban írták le először, mint a csontvelőben található, in vitro kultúrában a tenyésztőedény falához tapadva növekedő, fibroblastszerű morfológiát mutató, kolóniaképző sejteket. Terápiás megítélésük az utóbbi években óriási fejlődésen ment keresztül annak köszönhetően, hogy számos preklinikai és klinikai kísérlet bizonyította hatékonyságukat egyes betegségek kezelésében.
Az MSC-k sokfélesége és főbb tulajdonságai
MSC-k legnagyobb mennyiségben, mint „stroma” őssejtek a csontvelőben (CSV-MSC) találhatók meg a hematopoetikus őssejtek (HSC) mikrokörnyezeteként, de ennél sokkal könnyebben hozzáférhető forrásuk lehet a zsírszövet vagy a köldökzsinór Wharton-kocsonyája (WJ-MSC). Az International Society for Cellular Therapy (ISCT) három pontban foglalta össze az MSC-k közös jellemzőit:
• a tenyésztőedény aljához kitapadva növekednek (adherencia) és fibroblastszerű morfológiát mutatnak;
• kifejezik a CD73, CD90, CD105 sejtfelszíni markereket, de nem hordoznak semmilyen vérképző őssejtekre, vérsejt-fejlődési vonalakra, ill. endothel sejtekre jellemző markereket (CD45, CD34, CD14, CD11b, CD79α, CD19, CD31);
• képesek csont-, porc- és zsírsejtekké differenciálódni in vitro körülmények között.
A rendelkezésre álló adatok szerint a WJ-MSC-k számos előnnyel bírnak a CSV-MSC-vel szemben: kinyerésükhöz nincs szükség fájdalmas CSV-aspirációra, és viszonylag nagy számban kinyerhetők a Wharton-kocsonyából; ráadásul a WJ-MSC-k fiatalabb sejtvonalakat képviselnek, hiszen felületükön embrionális markereket is kifejeznek. A WJ-MSC-k jobban szaporíthatók laboratóriumi körülmények között és plasztikusabb sejtformák, mint a BM-MSC-k.
Az MSC-k hipoimmunogén, gyulladáscsökkentő és immunszuppresszív tulajdonsága
Az MSC-k hipoimmunogén tulajdonsága – amely az allogén, sőt a xenogén transzplantációk esetén elmaradó immunválaszt jelent – azzal magyarázható, hogy felületükön nem fejeznek ki MHC II, ill. csak kis mennyiségben fejeznek ki MHC I antigéneket. Ebből adódóan a betegek kezelése nem igényel autológ MSC-t, és elvileg bármely egészséges donor MSC-je felhasználható terápiák indítására.
Az ischaemiás vagy sérült szövetek szinte „vonzzák” a mesenchymalis őssejteket. A folyamat hátterében a felületükön található, a sejtek migrációjában fontos szerepet betöltő kemokin receptorok állnak. Az MSC-k is sokféle biológiailag aktív mediátort termelnek, amelyek direkt vagy indirekt úton közreműködnek a regeneráció folyamatában. A gyulladás helyszínén pl. az MSC-k olyan molekulákat bocsátanak ki, amelyek lokális gyulladáscsökkentő tulajdonságúak.
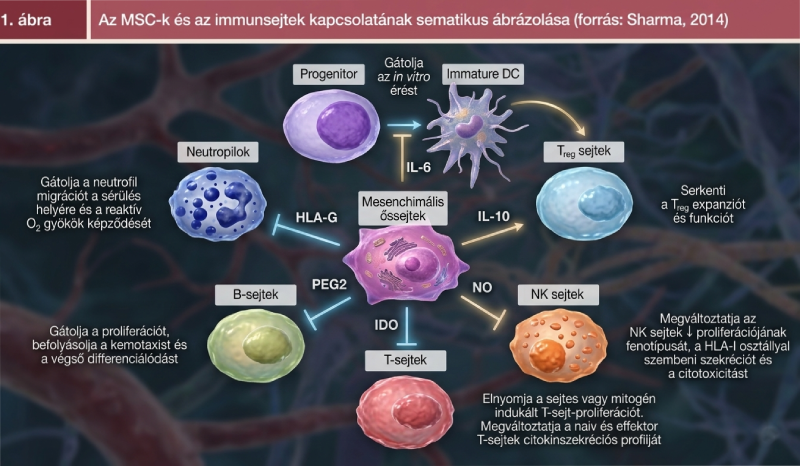
A mesenchymalis őssejtek gátolják az immunválaszban fontos szerepet betöltő T-, B-, NK-, antigénprezentáló sejtek aktivitását, egyes T-helper sejtek apoptózisát idézik elő és fokozzák az immunválaszt gátló regulátor T-sejtek osztódását. A részletesebben feltárt kapcsolataikat az 1. ábra foglalja össze.
2004-ben Le Blanc és mtsai első alkalommal számoltak be az MSC-k in vivo gyulladásgátló és immunszuppresszív hatásán alapuló sikeres terápiás beavatkozásról. Egy 9 éves – akut lymphoid leukaemia miatt allogén csontvelő-transzplantációval kezelt – kisfiúnál kialakult rendkívül súlyos (IV. stádiumú) akut graft versus host (aGVHD) betegséget kezeltek édesanyjától származó CSM-MSC-k többszöri adásával.
Klinikai kísérletek MSC-vel
1995 óta folynak klinikai kísérletek különböző eredetű mesenchymalis sejtekkel, párhuzamosan azokkal az alapkutatásokkal, amelyek a hatásmechanizmusuk tisztázására irányulnak. Míg 2012-ben 218 klinikai kísérlet folyt különböző eredetű MSC-vel, addig napjainkban 254, amelyekből 89 esetben köldökzsinórból izolált sejtekkel történik a kezelés. Egy korábbi cikkünkben bemutattuk ezeket a klinikai kísérleteket, kiemelve a porc és a máj regenerálásában, valamint a GVHD kezelésében folyó klinikai kísérletek kimagasló arányát.
Napjainkban a WJ-MSC sejtekkel folyó kísérletek még szélesebb skálán mozognak: egyes autoimmun betegségek (1-es típusú diabetes mellitus, sclerosis multiplex, szisztémás lupus) mellett, izomdisztrófia és az Alzheimer-kór kezelésére is folynak klinikai kísérletek. Néhány – az aGVHD megelőzését és a már kialakult betegség visszaszorítását, valamint néhány autoimmun betegség (Crohn-betegség, rheumatoid arthritis) kezelését célzó – „trial” azonban már eljutott a III. fázisba. Preklinikai stádiumban vannak a legkülönbözőbb daganatos betegségek, perifériális idegkárosodás, kardiovaszkuláris szövetek regenerációjára, ill. a 2-es típusú cukorbetegség kezelésére irányuló vizsgálatok. Azt, hogy ezek közül melyek lépnek a klinikai kísérletek közé, nem lehet megjósolni, mint ahogyan az is kérdéses, hogy mely klinikai kísérletek válnak rutin terápiás gyakorlattá.
Az MSC-k szerepe az ALS kezelésében
Az ALS (amyotrophis lateral sclerosis) a motoneuron-betegségek leggyakoribb fajtája, amely a mozgatóidegek pusztulása miatt az izmok gyengüléséhez, sorvadásához és a mozgásképtelenség miatt fellépő szövődmények miatt halálhoz vezet. A feltételezett okok között szerepelnek mutációk, extracelluláris faktorok, a nem idegi „support” sejtek és az immunrendszer hibái. Az ALS ma még nem teljesen ismert mechanizmusának feltárása érdekében számos állatkísérletet végeztek, és 2003 óta vizsgálják a mesenhymalis őssejtekkel történő kezelés lehetőségét is: Marconi és mtsai zsírszövetből származó MSC-t ültettek SOD1 mutációt hordozó transzgenikus egerekbe és bebizonyították, hogy a transzplantáció 4–6 héttel késleltette a motoros készségek romlását. Uccelli és mtsai a motoros készségek javulását, a testsúly csökkenésének lelassulását, valamint a túlélés javulását mutatták ki 17 nappal a beadás után, ALS egereken.
Az első humán klinikai kísérleteket Mazzini és mtsai végezték: a vizsgálat 9 betegre terjedt ki, amely során saját CSV-ből származó MSC-t alkalmaztak nem egységesített mennyiségben a betegek gerincvelőjébe történő injektálás formájában. Klinikai javulás nem volt tapasztalható, de nem észleltek mellékhatást sem. A vizsgálatokat később megismételték 10 további beteg esetében. Nem tapasztalták az ALS progressziójának lassulását, de felgyorsulását sem és a kezelést biztonságosnak és jól tolerálhatónak minősítették.
Karussis és mtsai autológ CSV-i eredetű MSC-t használtak 19 beteg esetén. Néhány alkalommal a sejteket szupermágneses vas-oxiddal jelölték. A betegek 6-tól 25 hónapig tartó megfigyelése során nem fordult elő késői mellékhatás, és a legtöbb beteg esetében a klinikai állapot stabilizálódását vagy enyhe javulását figyelték meg. A jelölt sejteket kapott betegek MRI-vizsgálata kimutatta, hogy az agyi területen beadott sejtek a harmadik agykamrába és a subarachnoidealis térbe jutottak át és igazolták az MSC-k immunmoduláló hatását már 4 órával a sejtek bejuttatása után.
ALS kezelés a Famicord Csoportban
A Famicord Csoport kezelési metódusa arra épül, hogy a WJ-MSC őssejteket nagyobb proliferatív potenciál jellemzi, mint a CSV eredetűeket. A KRIO Intézet – a Famicord Csoport magyar tagja – 2013-ban szabadalmat nyújtott be a WJ MSC-k izolálására és feldolgozására vonatkozólag. Ezen izolálási és feldolgozási elveket figyelembe véve a Famicord Csoport lengyel tagja, a Lengyel Őssejtbank (PBKM) 2014 októberében megkapta az orvosetikai hozzájárulást az ALS-betegek lengyelországi kezelésére. Az MSC-k első lengyelországi alkalmazása veleszületett neurológiai betegségek kezelésében a poznani Orvostudományi egyetem Bioetikai Bizottságának határozata (1141/12) alapján 2014 májusa óta folyamatosan zajlik.
Összefoglalás
Számos tanulmány és klinikai kísérlet foglalkozik a mesenchymalis őssejtek és ezen belül a köldökzsinór eredetű MSC-k gyakorlati jelentőségének megismerésével, amelyről áttekintést a www.clinicaltrials.gov ad. Az itt regisztrált kísérletek folyamatosan növekvő száma és sokfélesége arra enged következtetni, hogy bár korábban elsősorban a regeneratív orvoslás eszközeként jellemezték őket, napjainkban egyes autoimmun betegségek ill. aGVHD kezelése mellett az ALS kezelésében is jelentős szerepet kaphatnak.
Balogh I., Száraz L.
HIVATKOZÁSOK
- Gluckman E, Broxmeyer HA, Auerbach AD, et al. Hematopoietic reconstitution in a patient with Fanconi’s anemia by means of umbilical-cord blood from an HLA-identical sibling. New England Journal of Medicine. 1989;321:1174–8.
- Friedenstein AJ, Petrakova KV, Kurolesova AI, et al. Heterotopic transplants of bone marrow. Transplantation. 1968;6:230–247.
- Dominici M, Le Blanc K, Mueller I, et al. Minimal criteria for defining multipotent multipotent mesenchymal stromal cells. The international Society for Cellular Therapy position statement. Cytotherapy. 2006;8:314–317.
- Sharma R, Pollock K, Hubel A, et al. Mesenchymal stem or stromal cells: a review of clinical applications and manufacturing practices. Transfusion. 2014;54:1418–1437.
- Mundra V, Gerling IC, Mahato RI. Mesenchymal stem cell-based therapy. Molecular Pharmaceutics. 2013;10:77–89.
- Blanc KL, Rasmusson I, Sundberg B, et al. Treatment of severe acute graft-versus-host disease with third party haploidentical mesenchymal stem cells. Lancet. 2004;363:1439–41.
- Száraz L, Kocsis A, Fűrész K, et al. Köldökzsinór eredetű mesenchymalis őssejtek jellemzése, várható terápiás felhasználása. Nőgyógyászati és Szülészeti Továbbképző Szemle. 2013;15:114–116.
- https://clinicaltrials.gov/ct2/results?term=umbilical+cord+mesenchymal+stem+cell; hozzáférés időpontja: 2015.02.04.
- Watson N, Divers R, Kedar R, et al. Discarded Wharton jelly of the human umbilical cord: a viable source for mesenchymal stromal cells. Cytotherapy. 2015;17:18–24.
- Lewis M, Suzuki M. Therapeutic applications of mesenchymal stem cells for amyotrophic lateral sclerosis. Stem Cell Research & Therapy. 2014;5:32.
- Marconi S, Bonaconsa M, Scambi I, et al. Systemic treatment with adipose-derived mesenchymal stem cells ameliorates clinical and pathological features in the amyotrophic lateral sclerosis murine model. Neuroscience. 2013;248:333–43.
- Uccelli A, Milanese M, Principato MC, et al. Intravenous mesenchymal stem cells improve survival and motor function in experimental amyotrophic lateral sclerosis. Mol. Med. 2012;18:794–804.
- Mazzini L, Ferrero I, Luparello V, et al. Mesenchymal stem cell transplantation in amyotrophic lateral sclerosis: A Phase I clinical trial. Exp Neurol. 2010;223:229–37.
- Karussis D, Karageorgiou C, Vaknin-Dembinsky A, et al. Safety and immunological effects of mesenchymal stem cell transplantation in patients with multiple sclerosis and amyotrophic lateral sclerosis. Arch Neurol. 2010;67:1187–94.
Értékelje a cikket:










